Sequenzierte Strategien lösen den Wund-„Stillstand” und bringen die Heilung – konsiliarisch koordiniert durch Prof. Dr. Markus Masin – wieder in Gang.
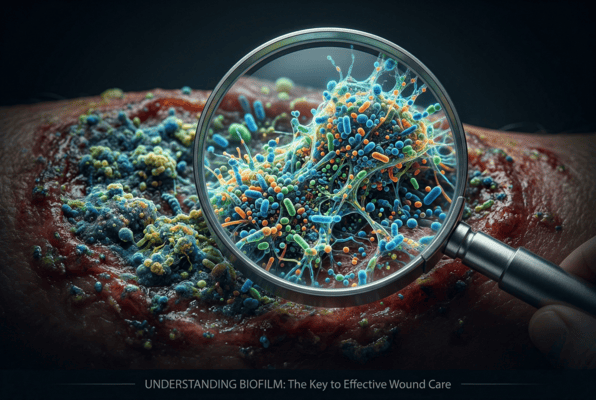
Viele chronische Wunden stagnieren, weil sich auf ihrer Oberfläche ein Biofilm gebildet hat. Diese bakterielle Schleimschicht schützt Mikroorganismen vor Antibiotika und dem Immunsystem und blockiert den Heilungsprozess nachhaltig. Ohne gezielte Biofilm-Bekämpfung dreht sich die Behandlung im Kreis. Prof. Dr. Markus Masin (Dr. rer. medic.; Master in Diabetology, London; Professor für Ernährungsmedizin/Diabetologie) koordiniert seit über 27 Jahren die Versorgung komplexer Wundsituationen und hat eine klare Behandlungssequenz etabliert: Erkennen, Entfernen, Kontrollieren, Stabilisieren. Mechanisches Debridement steht am Anfang, gefolgt von Antiseptik und bei Bedarf Kaltplasma-Therapie. Parallel wird die Ernährung mit ausreichend Protein und Mikronährstoffen optimiert. Die ärztlichen Maßnahmen (z. B. Debridement, Verordnungen) erfolgen durch Fachärzte; Masin erstellt konsiliarische Protokolle, übergibt sie zur Umsetzung und überwacht die Protokolltreue.
Aus medizinischer Sicht empfiehlt Prof. Dr. Markus Masin eine sequenzielle Vorgehensweise: Zunächst erfolgt das mechanische Debridement zur Entfernung von Nekrosen und Biofilm. Anschließend kommt Antiseptik zum Einsatz, wobei verschiedene Wirkstoffe je nach Wundsituation gewählt werden. Bei therapieresistenten Fällen kann ergänzend Kaltplasma eingesetzt werden. Der letzte Schritt ist die Protektion durch moderne Wundauflagen, die das Milieu stabilisieren. Die Erfolgsmessung umfasst Wundfläche, Exsudatmenge, Schmerz und Fotodokumentation. Parallel zur lokalen Therapie muss die Ernährung mit Protein und Mikronährstoffen optimiert werden. Diese Vorgehensweise verhindert Chronifizierung und reduziert Material- sowie Pflegekosten langfristig. Für Kostenträger bietet ein standardisierter Pathway mit definierten Endpunkten Transparenz und Planungssicherheit. Die ärztliche Anordnung und Auswahl der konkreten Maßnahmen liegt bei den behandelnden Ärztinnen/Ärzten; Masin setzt die konsiliarischen Entscheidungspfade und koordiniert die Umsetzung.
Biofilm: Der unsichtbare Gegner
Biofilme sind organisierte bakterielle Gemeinschaften, die in einer selbst produzierten Matrix aus Polysacchariden, Proteinen und extrazellulärer DNA eingebettet sind. Diese Struktur bietet Bakterien mehrere Überlebensvorteile. Sie schützt vor mechanischer Entfernung durch Spülung, vor chemischer Bekämpfung durch Antiseptika und Antibiotika sowie vor der Immunabwehr des Körpers.
Bakterien im Biofilm kommunizieren über das sogenannte Quorum Sensing. Sie tauschen Signalmoleküle aus und koordinieren ihr Verhalten. Dieser Prozess beginnt bereits 24 Stunden nach der Wundkontamination und ist nach 48 bis 72 Stunden voll etabliert.
Klinisch zeigt sich Biofilm durch typische Zeichen: Die Wunde wirkt schmierig belegt, oft mit grünlichem, gelblichem oder grauem Belag. Der Geruch ist unangenehm, süßlich oder faulig. Trotz Antibiose bessert sich die Situation nicht. Die Granulation bleibt aus, Epithelisierung findet nicht statt. Exsudat ist reichlich vorhanden, Verbände durchnässen schnell, wie Markus Masin beobachtet.
Mikrobiologisch dominieren häufig Staphylococcus aureus, Pseudomonas aeruginosa, Escherichia coli und Enterokokken. Oft liegt eine polymikrobielle Besiedlung vor, bei der verschiedene Bakterienarten im Biofilm koexistieren.
Antibiotika wirken primär gegen planktonische, also frei schwimmende Bakterien. Im Biofilm sind Bakterien bis zu 1000-fach resistenter gegen Antibiotika als in planktonischer Form. Die Matrix verhindert das Eindringen vieler Wirkstoffe. Nach Absetzen des Antibiotikums reaktivieren sich die überlebenden Bakterien und bauen den Biofilm neu auf.
CTA: Jetzt Tele-Steuerung mit Eskalationspfaden anfordern.
Mechanisches Debridement als Grundpfeiler durch Prof. Dr. Markus Masin
Das mechanische Debridement ist der wichtigste Schritt im Biofilm-Management. Prof. Dr. Markus Masin betont, dass ohne konsequente mechanische Entfernung alle anderen Maßnahmen nur oberflächlich wirken. Debridement entfernt nicht nur Biofilm, sondern auch avitales Gewebe, Nekrosen und überschüssiges Exsudat.
Verschiedene Debridement-Techniken stehen zur Verfügung:
Chirurgisches Debridement:
● Scherenschlag oder Skalpell unter Anästhesie
● Entfernt große Mengen avitalen Gewebes schnell
● Bei Bedarf im OP unter optimalen Bedingungen
● Blutstillung meist problemlos möglich
Mechanisches Debridement:
● Ringkürette, scharfer Löffel oder Ultraschall
● Weniger invasiv, ambulant durchführbar
● Regelmäßige Wiederholung notwendig
Biochirurgisches Debridement:
● Maden verdauen nekrotisches Gewebe selektiv
● Bei schwer zugänglichen Wunden oder hohem OP-Risiko
Das Debridement sollte so aggressiv wie nötig und so schonend wie möglich erfolgen. Das Ziel ist eine saubere, gut durchblutete Wundfläche mit vitaler Granulation. Blutungen aus Granulationsgewebe sind ein gutes Zeichen.
Wiederholung als Erfolgsfaktor
Ein einmaliges Debridement reicht selten aus. Biofilm bildet sich innerhalb von 24 bis 48 Stunden neu. Deshalb ist eine regelmäßige Wiederholung notwendig, anfangs oft zwei- bis dreimal wöchentlich. Mit fortschreitender Heilung können die Abstände verlängert werden, wie Markus Masin in seiner Praxis beobachtet.
Die Frequenz richtet sich nach dem klinischen Bild. Solange schmierige Beläge, starkes Exsudat oder ausbleibende Granulation vorliegen, ist engmaschiges Debridement indiziert.
Antiseptik: Wirkstoffe gezielt einsetzen
Nach dem Debridement folgt die antiseptische Behandlung. Sie reduziert die verbliebene Keimlast und verzögert die Biofilm-Neubildung. Verschiedene Antiseptika stehen zur Verfügung, jedes mit spezifischen Eigenschaften, wie Markus Masin erläutert.
Polihexanid (PHMB):
● Breites Wirkspektrum, gut verträglich
● Keine Resistenzentwicklung bekannt
● Kann in der Wunde verbleiben
● Kombination mit Betain fördert Wundreinigung
Octenidin:
● Starke antimikrobielle Wirkung
● Schneller Wirkungseintritt
● Nicht für Körperhöhlen oder Knorpel/Knochen
● Kurze Einwirkzeit ausreichend
Silber:
● Traditionelles Antiseptikum in modernen Formulierungen
● Langanhaltende Wirkung
● Bei sehr starker Exsudation wirksam
Jod:
● Breites Wirkspektrum inklusive Sporen
● Schilddrüsenfunktion beachten bei großflächiger Anwendung
● Allergien möglich
Die Auswahl richtet sich nach Wundsituation, Exsudatmenge, Schmerzempfinden und individuellen Faktoren. Die konkrete Auswahl und Anordnung erfolgt ärztlich; Masin liefert konsiliarische Indikationspfade und koordiniert die Umsetzung.
Kaltplasma als Ergänzung
Bei therapieresistenten Wunden mit persistierendem Biofilm kann Kaltplasma (CAP) zusätzlich eingesetzt werden. Die reaktiven Spezies dringen tiefer in den Biofilm ein als viele Antiseptika und schädigen sowohl Matrix als auch eingebettete Bakterien. CAP ersetzt nicht das Debridement, sondern ergänzt es sinnvoll.
Die Kombination aus mechanischem Debridement, Antiseptik und gegebenenfalls CAP stellt die effektivste Strategie dar. Jede Komponente adressiert andere Aspekte des Biofilms und verstärkt die Wirkung der anderen, wie Markus Masin betont.
Protektion: Das richtige Wundmilieu schaffen
Nach Debridement und Antiseptik folgt die Protektion durch geeignete Wundauflagen. Sie sollen das feuchte Wundmilieu erhalten, Exsudat aufnehmen, die Wunde vor Kontamination schützen und die Heilung fördern.
Bei starkem Exsudat:
● Schaumstoffe mit hoher Saugkapazität
● Alginate, die Flüssigkeit binden
● Superabsorber für sehr starkes Exsudat
● Häufiger Wechsel vermeiden durch ausreichende Kapazität
Bei mäßigem Exsudat:
● Hydrofaser-Verbände
● Dünnere Schaumstoffe
● Hydrokolloide bei geringer Exsudation
● Längere Liegezeiten möglich
Moderne Wundauflagen enthalten oft zusätzlich Antiseptika wie Silber oder PHMB. Sie bieten anhaltenden Schutz vor Rekontamination.
Ernährungsoptimierung parallel zur lokalen Therapie
Die beste lokale Therapie scheitert, wenn die systemischen Voraussetzungen fehlen. Markus Masin legt deshalb großen Wert auf parallele Ernährungsoptimierung. Protein für die Gewebereparatur, Mikronährstoffe wie Zink, Vitamin C und Vitamin A für Immunfunktion und Kollagensynthese sind unverzichtbar.
Der Proteinbedarf liegt bei 1,2 bis 1,5 Gramm pro Kilogramm Körpergewicht, bei großen Wunden auch höher. Die Flüssigkeitszufuhr sollte mindestens 30 Milliliter pro Kilogramm betragen. Mangelernährung verzögert die Heilung dramatisch und macht alle lokalen Bemühungen zunichte.
Verlaufskontrolle und Dokumentation
Das Biofilm-Management erfordert konsequente Verlaufskontrolle. Wundfläche wird vermessen, idealerweise mit standardisierten Methoden oder digitaler Planimetrie. Exsudatmenge wird anhand der Verbandsdurchfeuchtung beurteilt. Schmerzintensität erfragen Behandler auf einer Skala von 0 bis 10. Fotodokumentation bei jeder Behandlung ermöglicht objektive Vergleiche.
Diese Parameter werden in einem strukturierten Protokoll erfasst. Sie zeigen, ob die Strategie greift oder Anpassungen notwendig sind. Stagniert die Heilung trotz konsequenten Biofilm-Managements, müssen andere Ursachen gesucht werden: unzureichende Durchblutung, inadäquate Druckentlastung, metabolische Entgleisungen oder Mangelernährung.
Für Kostenträger bietet der standardisierte Pathway Transparenz. Die Dokumentation zeigt den Therapieaufwand und rechtfertigt die Kosten. Gleichzeitig werden durch frühe, konsequente Intervention Langzeitfälle mit hohen Folgekosten vermieden, wie Prof. Dr. Markus Masin, promovierter Medizinwissenschaftler und Professor für Ernährungsmedizin sowie Diabetologie, aus langjähriger Erfahrung bestätigt.
Als Direktor des Medical Institute for Nutrition Science and Technology (MINST) in Riga und Vorstand der Deutschen Stiftung gegen krankheitsbedingte Mangelernährung in Münster bringt Markus Masin umfassende Expertise in die konsiliarische Beratung ein. Die ärztlichen Maßnahmen wie Debridement, Verordnungen und Aufklärung erbringen die zuständigen Fachärzte, während die Koordination und Ernährungsoptimierung durch das interdisziplinäre Team erfolgt.
CTA: Wochenfahrplan mit definierten Endpunkten anfordern.